-Los elementos químicos están formados por partículas muy pequeñas e individuales llamadas átomos.
-Los átomos del mismo elemento son iguales tanto en masa como en el resto de sus propiedades.
-Los átomos de elementos diferentes son diferentes en su masa y en el resto de sus propiedades.
-Los átomos de elementos diferentes se unen entre sí para formar compuestos.
Esta teoría fue enunciada en el siglo XIX.
Naturaleza eléctrica de las cargas:
Los fenómenos de atracción y de repulsión muestran que existen dos tipos de cargas: una negativa y otra positiva.
-Fuerza de repulsión: las cargas eléctricas de igual signo se repelen.
Partículas subatómicas: son las partículas más pequeñas que encontramos en le átomo, las tres partículas subatómicas que mayor importancia tiene son : los protones, los neutrones y los electrones.
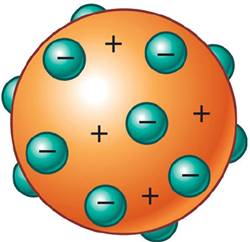
Modelo atómico de Thomson: este señor imaginó el átomo como una pequeña esfera uniforme cargada positivamente en la que estaban incrustados los electrones e un número tal que el conjunto era eléctricamente positivo.
Tipos de iones:
-Catión: es un ion con carga positiva que se forma cuando un átomo o grupo de átomos pierde algún electrón.
-Anión: es un ion con carga negativa que se forma cuando u átomo o grupo de átomos gana algún electrón.
 Modelo atómico de Rutherford: imaginó al átomo con una pequeña zona interior, con mucha masa y carga positiva, a la que mamó núcleo, y en la que se encontrarían los protones, y una corteza exterior, que se encontraría a gran distancia del núcleo.
Modelo atómico de Rutherford: imaginó al átomo con una pequeña zona interior, con mucha masa y carga positiva, a la que mamó núcleo, y en la que se encontrarían los protones, y una corteza exterior, que se encontraría a gran distancia del núcleo.
El modelo atómico de Bohr: Bohr ideó un nuevo modelo atómico en el que se solventaba los problemas del modelo de Rutherford, en el se podía explicar por que los electrones al girar no se caían sobre el núcleo y por que se producían espectros.
Tipos de uniones:
-Unión covalente
-Unión iónica
-Unión metálica


No hay comentarios:
Publicar un comentario